
Forschung
Unsere Forschungsgruppe konzentriert sich auf das Design von Elektronenrelais zur Überbrückung von Redox-Proteinen und Elektroden für Energieumwandlung und Energiesparmaßnahmen. Redox-Enzyme sind hochaktive und selektive Katalysatoren für verschiedene Reaktionen und damit attraktiv für technologische Anwendungen. Wir verwenden synthetische Chemie, um Redox-Schnittstellen auf der Elektrodenoberfläche zu bilden, um die Ziel-Biomoleküle in Bezug auf ihre Eigenschaften und Anwendungszwecke anzupassen. Unsere Hauptprojekte sind Biosensorik, Biophotovoltaik, Biokraftstoffzellen und Bioelektrokatalyse.
Projekte
Biobrennstoffzellen
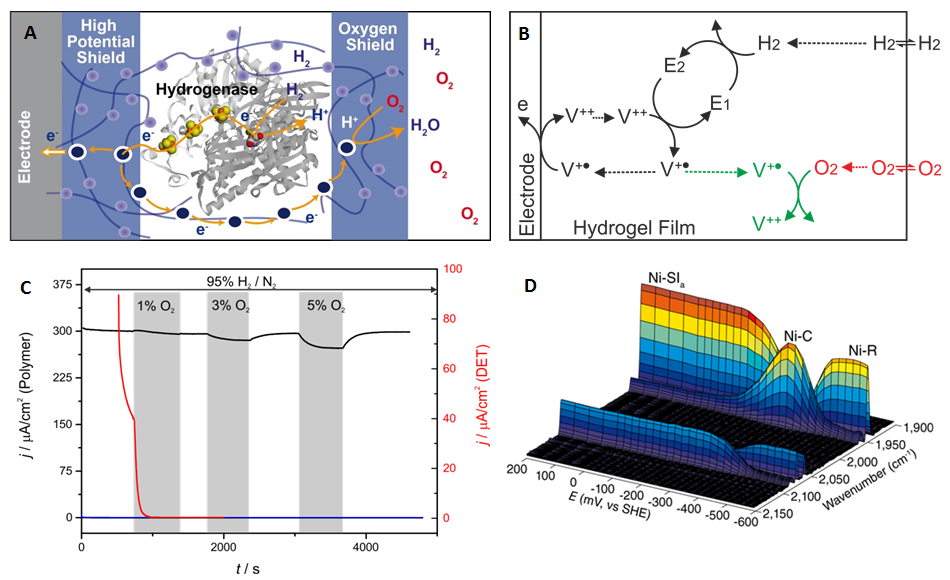 Wir setzen unsere Expertise in Chemie und Elektrochemie ein, um neue Strategien zu entwickeln, um empfindliche Katalysatoren vor den rauen Bedingungen zu schützen, die in Brennstoffzellen und anderen technologischen Geräten im Betrieb herrschen2. Bisher haben nur Materialien auf Edelmetallbasis technologische Anwendungen erreicht. In Zusammenarbeit mit W. Schuhmann, O. Rüdiger und W. Lubitz haben wir ein Redox-Hydrogel entwickelt, das als Schutzmatrix für den Katalysator dient3. Das Konzept wurde erfolgreich mit einer Hydrogenase als Modell für einen effizienten Wasserstoffoxidationskatalysator mit extremer Empfindlichkeit demonstriert. Das in Nature Chemistry berichtete Hydrogel-Konzept eröffnet die Möglichkeit, eine Vielzahl anderer empfindlicher biologischer oder künstlicher Katalysatoren zu integrieren, bei denen die intrinsische Stabilität nicht weiter erhöht werden kann. Dies ist ein wichtiger Schritt hin zu einem neuartigen Brennstoffzellen-Redesign, das sie im Wettlauf um eine globale nachhaltige Energieversorgung an die Spitze bringen könnte.
Wir setzen unsere Expertise in Chemie und Elektrochemie ein, um neue Strategien zu entwickeln, um empfindliche Katalysatoren vor den rauen Bedingungen zu schützen, die in Brennstoffzellen und anderen technologischen Geräten im Betrieb herrschen2. Bisher haben nur Materialien auf Edelmetallbasis technologische Anwendungen erreicht. In Zusammenarbeit mit W. Schuhmann, O. Rüdiger und W. Lubitz haben wir ein Redox-Hydrogel entwickelt, das als Schutzmatrix für den Katalysator dient3. Das Konzept wurde erfolgreich mit einer Hydrogenase als Modell für einen effizienten Wasserstoffoxidationskatalysator mit extremer Empfindlichkeit demonstriert. Das in Nature Chemistry berichtete Hydrogel-Konzept eröffnet die Möglichkeit, eine Vielzahl anderer empfindlicher biologischer oder künstlicher Katalysatoren zu integrieren, bei denen die intrinsische Stabilität nicht weiter erhöht werden kann. Dies ist ein wichtiger Schritt hin zu einem neuartigen Brennstoffzellen-Redesign, das sie im Wettlauf um eine globale nachhaltige Energieversorgung an die Spitze bringen könnte.
- Plumeré N., Rüdiger O., Alsheikh Oughli A., Williams R., Vivekananthan J., Pöller S., Schuhmann W., Lubitz W. Nature Chemistry, 2014, 6, 822–827. DOI: 10.1038/nchem.2022
- Alsheikh Oughli A., Conzuelo F., Winkler M., Happe T., Lubitz W., Schuhmann W., Rüdiger O., Plumeré N. Angew. Chem. Int. Ed., 2015, 54 (42), 12329–12333. DOI: 10.1002/anie.201502776
- Fourmond V., Stapf S., Li H., Buesen D., Birrell J., Olaf R.; Lubitz W., Schuhmann W., Plumeré N., Léger C. J. Am. Chem. Soc., 2015, 137, 5494-5505. DOI: 10.1021/jacs.5b01194
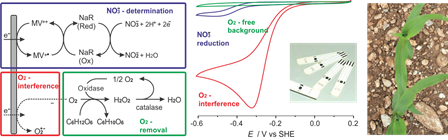
Nitrat Biosensor
Die Auswirkungen der Nitratbiosensorik auf die Schonung fossiler Ressourcen und die Reduzierung von CO2-Emissionen wurden kürzlich von der KlimaExpo.NRW erkannt, die es zu einem Schwerpunktthema machte, den Klimaschutz zu fördern und aufzuklären6. Das Verfahren wartet auf die Validierung einer anhängigen Patentanmeldung7.
- Plumeré N. Nachrichten aus der Chemie 2014, 62(7), 777-779. DOI: 10.1002/nadc.201490261
- Campbell W. H., Henig J., Plumeré N. Bioelectrochemistry, 2013, 93, 46-50. DOI: 10.1016/j.bioelechem.2012.07.002
- Plumeré N. Analytical and Bioanalytical Chemistry, 2013, 405(11), 3731-3738. DOI: 10.1007/s00216-013-6827-z
- Swoboda M., Henig J., Cheng H.-M., Brugger D., Haltrich D., Plumeré N., Schlierf M. ACS Nano, 2012, 6(7), 6364-6369.DOI: 10.1021/nn301895c
- Plumeré N., Henig J. and Campbell W. H. Analytical Chemistry, 2012, 84, 2141-2146. DOI: 10.1021/ac2020883
- Plumeré N.,Nitratsensor: Schluss mit Überdüngung – Feldanalytik in der Landwirtschaft. KlimaExpo.NRW Motor für den Fortschritt
- Plumeré N., Campbell W. H., Campbell E. R., Systems and Methods for Enzymatic Oxygen Removal. US2012211372 (A1) – 2012-08-23
Biophotovoltaiks
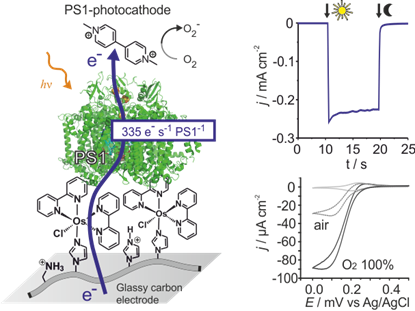
Zu diesem Zweck entwickeln wir Redox-Hydrogele für die hocheffiziente elektrische Kontaktierung und Stabilisierung des natürlichen photosynthetischen Proteins in künstlichen Geräten. Während frühe Vorrichtungen nur einen geringen Wirkungsgrad ergaben, führte die Feinabstimmung von Elektronenmediatoren mit Redoxpotentialen, die an das des Proteins angepasst waren, zu einer Verbesserung der beiden Photoströme4 und der Spannungen5 um mehrere Größenordnungen. Gemeinsam mit unseren Kooperationspartnern (W. Schuhmann, M. Nowaczyk und M. Rögner) haben wir gezeigt, dass Elektronen, die von photosynthetischen Proteinen bereitgestellt werden, an künstlichen Leitmaterialien noch schneller zurückgewonnen werden können als bei der natürlichen Photosynthese selbst4. Die Möglichkeit, diese Leistungen weiter zu verbessern, erhöht die Erwartung, dass biophotovoltaische Geräte schließlich einen praktischen Wirkungsgrad erreichen, um elektrische Energie sowohl in High-Tech-Geräten, wie biokompatible Photovoltaik in intelligenten Kontaktlinsen 6, als auch in Low-Tech-Großzellen, die „lackiert“ sind, bereitzustellen, was neue Wege für das Cost-per-Watt-Rennen in der elektrischen Energieerzeugung7 eröffnet.
- Plumeré, N. Nature Nanotech. 2012, 7 (10), 616–617. DOI: 10.1038/nnano.2012.175
- Zhao F., Conzuelo F., Hartmann V., Li H., Nowaczyk M. M., Plumeré N., Rögner M., Schuhmann W., J. Phys. Chem. B, 2015, 119 (43), 13726–13731. DOI: 10.1021/acs.jpcb.5b03511
- Kothe, T.; Plumeré, N.; Badura, A.; Nowaczyk, M. M.; Guschin, D. A.; Rögner, M.; Schuhmann, W., Angew. Chem. Int. Ed. 2013, 52 (52), 14233–14236. DOI: 10.1002/anie.201303671
- Kothe T., S. Pöller, F. Zhao, P. Fortgang, M. Rögner, W. Schuhmann, N. Plumeré Chemistry – A European Journal, 2014, 20, 11029–11034. DOI: 10.1002/chem.201402585
- Hartmann V.,Kothe T., Pöller S., El-Mohsnawy E., Nowaczyk M. M., Plumeré N., Schuhmann W.,Rögner M., Phys. Chem. Chem. Phys., 2014, 16, 11936-11941. DOI: 10.1039/C4CP00380B
- Ravilious K, Clothes that recharge your laptop – the near-endless possibilities of artificial leaves. Horizon, The research & innovation magazine of the European commission. 16 October 2014
- Plumeré et al., Researchers forecast an Ebola vaccine and low-cost solar cells in 2015. Horizon, The research & innovation magazine of the European commission, 5 January 2015
Kontrollierte Orientierung von redox-aktiven Enzymen auf Elektrodenoberflächen
Der direkte Elektronentransfer zwischen Redox-Proteinen und Elektroden ist ein grundlegendes Thema in der Bio-Elektrokatalyse, Bioelektronik, Biosensoren, Biokraftstoffzellen und der Nanobiotechnologie. Ziel unserer Forschung ist es, funktionale Oberflächen auf molekularer Ebene zu gestalten, um unsere Fähigkeit zur effektiven Kontrolle und Steuerung der elektrochemischen Aktivität von Biomolekülen zu verbessern.
Wir nutzen organische Chemie, Molekularbiologie und elektrochemische Ansätze, um biologisch-organische Hybridarchitekturen aufzubauen. Wir arbeiten an der Entwicklung von nanoskaligen Chelatoren, um die spezifische Erkennung und Orientierung eines Redox-Proteins zu erreichen. Unser Interesse ist es, grundlegende Informationen über die Chelatwirkung auf der supramolekularen Ebene zu gewinnen. Das Verständnis und die Anpassung der molekularen Erkennung zwischen Rezeptor und Gast in Kombination mit dem Design von Elektronenrelais zur Überbrückung von Redoxenzymen sind die Schlüsselfaktoren für eine kontrollierte Orientierung und einen schnellen Elektronentransfer. Wir wenden unsere Redox-Protein-Immobilisierungskonzepte für Sensing (Nitratbiosensoren) und Energieumwandlungsanwendungen (Bio-Photovoltaik und Bio-Brennstoffzellen) an.
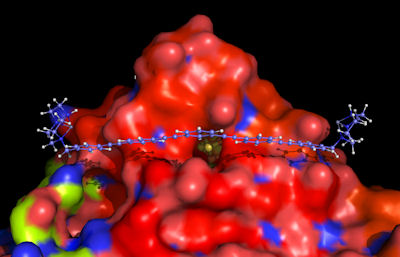
Figure 1: Ein Rezeptor-Gast Ensemble zwischen einer genetisch modifizierten Hydrogenase und einem nanometer großem starren Chelator.


